
LARUTAN ASAM, BASA DAN GARAM KLASIFIKASI MATERI DAN PERUBAHANNYA IPA SMP KELAS VII YouTube
Walaupun garam biasanya bersifat netral, namun bila dilarutkan dalam air, garam dapat menghasilkan larutan asam atau basa, tergantung pada kekuatan ion komponen mana yang lebih kuat. Jika kedua ion memiliki kekuatan yang sama, larutannya bersifat netral. Beberapa contoh garam yang mungkin tidak terkenal adalah: 1. Natrium klorida

Pengertian asam basa dan garam berserta contohnya PR Sekolahku
Jika Ka = Kb, maka garam tersebut bersifat netral. Jika Ka > Kb, maka garam tersebut bersifat asam. Jika Kb > Ka, maka garam tersebut bersifat basa. Pada reaksi hidrolisis, jumlah garam yang mengalami hidrolisis hanya sedikit, tetapi tetap menyebabkan perubahan nilai pH larutan. Karena itu reaksi hidrolisis juga disebut reaksi kesetimbangan.
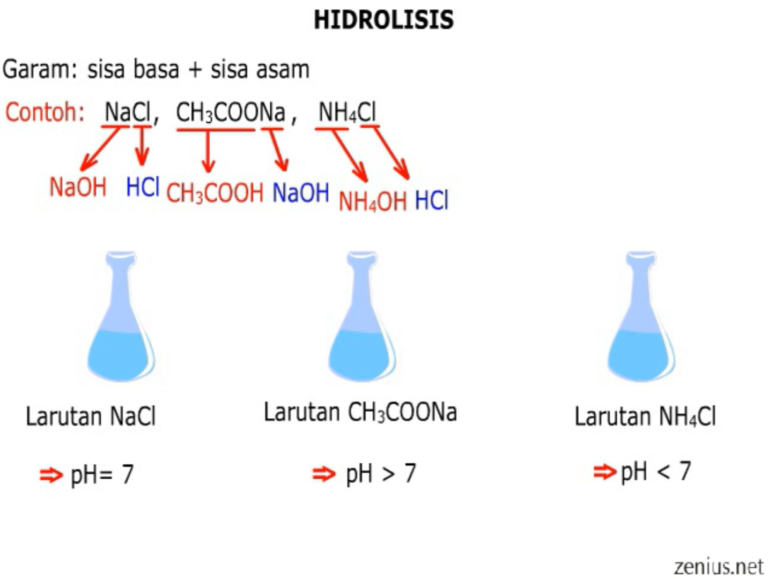
Pasangan Persamaan Reaksi Hidrolisis Untuk Garam Yang Bersifat Asam Adalah Homecare24
Garam yang terbentuk dari Asam Kuat dan Basa Lemah larutannya bersifat asam ( pH < 7 ). Misalnya; NH 4 Cl, FeCl 2, Al(NO 3) 3, dan lain-lain. Sedangkan garam yang terbentuk dari asam dan basa lemah sifat larutan tergantung dari derajat ionisasi asam dan basanya. Misalnya; (NH 4) 2 S, Fe 2 (CO 3) 3, AlPO 4, dan lain-lain. LATIHAN SOAL

Pengertian Hidrolisis Garam Dan Jenis Garam Ilmusaku
10 Contoh Garam Netral. Litium Klorida = LiCl. Litium Nitrat = LiNO 3. Litium Sulfat = Li 2 SO 4. Natrium Klorida = NaCl. Natrium Sulfat = Na 2 SO 4. Aluminium Flourida = AlF 3. Aluminium Sianida = Al (CN) 3.

TRIK MENENTUKAN GARAM TERHIDROLISIS SEBAGAIN BERSIFAT ASAM/BASA KIMIA OKE PINTAR
Larutan garam ini dapat bersifat asam, basa, maupun netral. Hal ini bergantung dari perbandingan kekuatan kation terhadap anion dalam reaksi dengan air. Memperjelas materi yang sebelumnya telah dijabarkan, contoh garam yang mengalami hidrolisis total atau sempurna adalah garam yang terbentuk dari asam lemah dan basa lemah.

Garam Kapal/Garam Yodium/Uyah Asin 500gram Lazada Indonesia
Asam + basa → garam + air. HCl + KOH → KCl + H2O. Garam dapur (NaCl) diperoleh dari air laut yang mengalami penguapan dan kristalisasi. Untuk menjadikannya garam beryodium, harus diproses iodisasi (garam kalium/KI). Sifat-sifat atau ciri-ciri garam: Larut dalam air. Contohnya : KNO3, NH4Cl, Na2SO4. Sukar larut dalam air.

Mengenal Proses Pembuatan Garam dari Air Laut Artha Garam Indonesia
Garam yang bersifat netral, memiliki pH = 7, berasal dari asam kuat dan basa kuat. Contoh: NaCl (natrium klorida), KI (kalium iodida), dan KNO 3 (kalium nitrat). Pengertian Larutan Garam, Sifat, Ciri, Jenis dan Contohnya : Adalah larutan yang didapat dari hasil reaksi asam dan basa. Garam merupakan suatu senyawa.

Garam Dapur Bermanfaat untuk Kecantikan?
1. Garam yang terbentuk dari komponen asam lemah dan basa kuat. Garam yang berasal dari asam lemah dan basa kuat dalam air akan mengalami hidrolisis sebagian. Komponen garam (anion asam lemah) mengalami hidrolisis menghasilkan sebuah ion OH -, maka pH > 7 sehingga larutan garam bersifat basa. Contoh. CH 3 COOK, CH 3 COONa, KCN, CaS.

PH hidrolisi atau garamsoal garam bersifat asam kimia SMA YouTube
Garam yang bersifat netral, memiliki pH = 7, berasal dari asam kuat dan basa kuat. Contoh: NaCl (natrium klorida), KI (kalium iodida), dan KNO 3 (kalium nitrat). garam dapur, NaCl → Na+ + Cl-besi sulfat, Fe2(SO4)3 → 2Fe3+ + 3SO3-4. Baca Juga Artikel Yang Mungkin Berhubungan : Pengertian Reaksi Kimia.

Mengenal Proses Pembuatan Garam Halus Artha Garam Indonesia
Reaksi kimia garam. Garam dapat terbentuk dari 4 reaksi kimia. Reaksi kimia adalah sebagai berikut: Garam dari asam kuat dan basa kuat, garam ini bersifat netral (pH = 7). Contohnya adalah NaCl, KCl, K 2 SO 4, Ca (NO 3) 2. Garam dari asam kuat dan basa lemah, garam ini bersifat asam (pH <7). Contohnya adalah Zn (ClO 4 )2, NH 4 Cl, AlCl 3, Fe.

•Pengertian Larutan Garam Epicologi Epicologi
Garam asam (Acidic salt) Jika asam polibasa dinetralkan sebagian oleh basa, garam yang terbentuk bersifat asam. Dengan kata lain, garam semacam itu dihasilkan dengan penggantian hanya sebagian dari hidrogen asam dari asam polibasa dengan logam. Yang termasuk garam jenis ini misalnya NaHSO 4, NaHS, NaHCO 3. Garam ganda (Double salt)

Garam yang Mengalami Hidrolisis Sebagian dan Bersifat Asam adalah? Blog Mamikos
Larutan Asam. Sangat mudah menemukan senyawa asam dalam beragam barang sehari-hari, termasuk pada makanan, minuman, atau cairan pembersih rumah. Jeruk, lemon, dan tomat merupakan contoh buah dan sayur yang mengandung asam. Cuka dapur sebagai penambah rasa juga mengandung asam asetat. Aki pada kendaraan bermotor terdiri dari asam sulfat.

10 Contoh Garam yang Digunakan dalam Kehidupan Seharihari Sains Kimia
Sehingga, hidrolisis garam adalah reaksi antara salah satu ion-ion garam (kation atau anion) dengan air dan membentuk larutan bersifat asam atau basa. Sifat asam atau basa larutan yang dihasilkan hidrolisis garam bergantung pada jenis asam basa yang membentuk garam tersebut. Baca juga: Hukum Kekekalan Energi: Pengertian, Rumus, dan Penerapannya
Jual Garam Refina Refined Salt Garam Dapur 500 gram Shopee Indonesia
Dalam ilmu kimia, garam adalah senyawa ionik yang terdiri dari ion positif dan ion negatif , sehingga membentuk senyawa netral (tanpa bermuatan). Garam terbentuk dari hasil reaksi asam dan basa. Komponen kation dan anion ini dapat berupa senyawa anorganik seperti klorida (Cl −), dan.

INFOGRAFIK Mengenal Manfaat Garam, Batas Aman hingga Bahayanya apabila Dikonsumsi Berlebih...
Salah satu senyawa garam paling umum adalah NaCl atau biasa dikenal dengan garam dapur yang biasa Sobat Pijar konsumsi sehari-hari itu. NaCl merupakan garam yang bersifat netral. Tapi, ternyata ada garam lain yang sifatnya asam serta basa, lho! Jadi, garam dapur bukanlah satu-satunya 'garam' di dunia ini.

PH Hidrolisis ( Garam ) yang bersifat basa Kimia SMA YouTube
Artinya, senyawa garam bukan hanya garam daput atau natrium klorida (NaCl). Melainkan, hampir semua senyawa ionik yang terbentuk dari anion dan kation. Baca juga: Ciri-ciri Senyawa Ionik. Jenis-jenis senyawa garam. Berdasarkan kelarutannya, senyawa garam dibedakan menjadi dua yaitu garam yang sukar larut dan garam yang mudah larut.